来源:研之成理
▲第一作者:王秀夷(南开大学);李迪迪(华东理工大学);高子睿(北京大学)
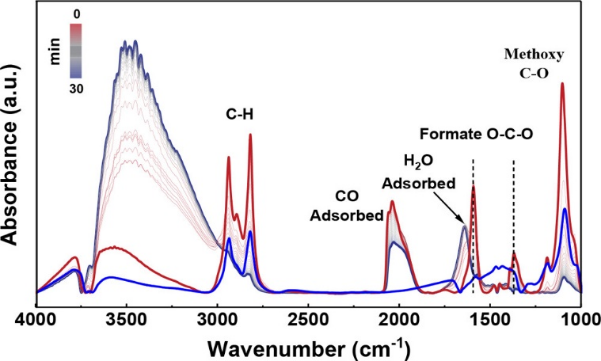
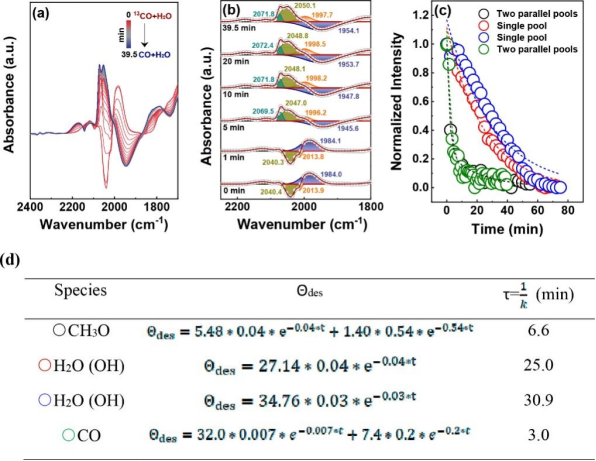
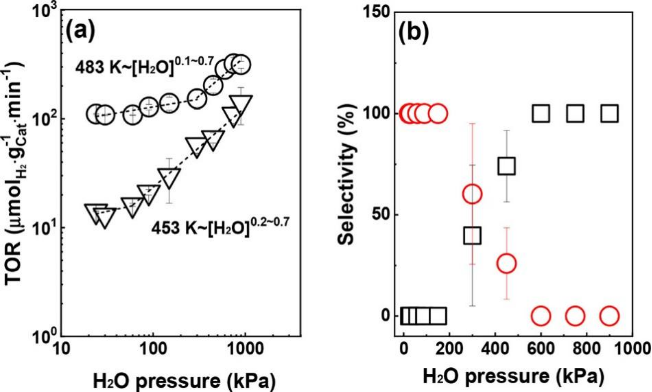
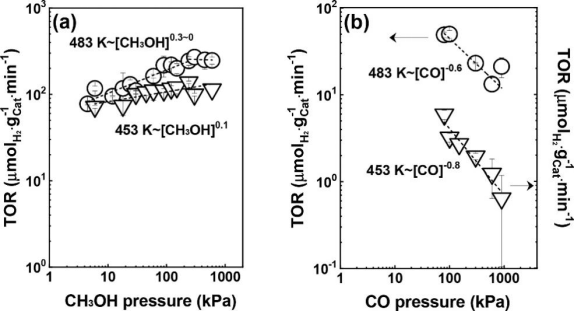
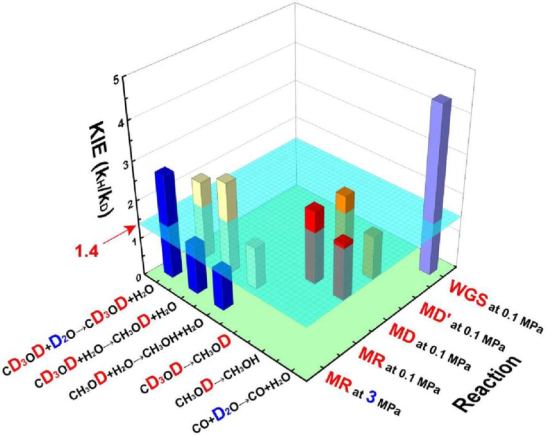
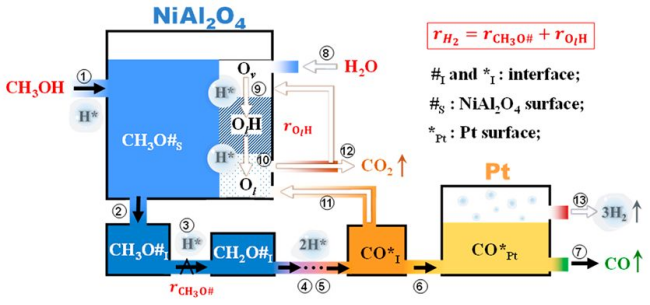
通讯作者:郭勇(华东理工大学);张洪波(南开大学);马丁(北京大学)近期,南开大学张洪波研究员、华东理工大学郭勇副研究员、北京大学马丁教授合作在J. Am. Chem. Soc.期刊上发表了题为“The Nature of Interfacial Catalysis over Pt/NiAl2O4 for Hydrogen Production from Methanol Reforming Reaction”的文章(DOI: 10.1021/jacs.2c09437)。该工作通过红外光谱结合稳态条件下的同位素瞬态交换实验(steady state isotopic transient kinetic analysis (SSITKA))、化学反应动力学和同位素取代实验,系统研究了甲醇分子以及水分子在催化剂表面的吸附、活化,并建立了一个集约化的串联反应模型(Langmuir-Hinshelwood模型)来准确描述该反应过程。研究表明,该反应首先经历甲醇脱氢生成一氧化碳的基元过程,随后发生水气变换反应(WGS),并经历两个单独的动力学相关步骤(KRS),即吸附在界面位置的甲氧基的C–H键断裂和OlH基团内的O–H键断裂(Ol:氧填充表面空位)基元步骤;这两个过程的反应速率同时受到表面主要吸附态物种(MASIs)的种类以及浓度影响,它们分别是吸附在NiAl2O4和Pt上的甲氧基和CO物种。由于界面位点和载体上的氧空位被认为是甲醇脱氢和WGS反应的活性位点,载体上吸附的甲氧基和Pt上吸附的CO物种的双向溢流过程被认为是该反应不可或缺的基元步骤。甲醇重整制氢可以帮助解决氢气储存和运输中存在的诸多限制,同时实现甲醇和水的高效活化是摆在科研工作者面前的重要难题,目前被广泛研究的催化体系包括金属/金属氧化物和金属/碳化物等。然而,相关反应机理(i.e. 包括活性组分以及反应历程)仍存在争议。▲图1 吸附在1 wt % Pt/NiAl2O4上的反应中间物种的红外光谱图(红色─:通入2 kPa CH3OH 0.5小时并以Ar吹扫后的红外谱图;海军蓝─:在吸附了甲醇之后的催化剂上持续通入2 kPa H2O 0.5小时后的红外谱图), 以及吸附在NiAl2O4上的反应中间物种的红外光谱图(蓝色─:通入2 kPa CH3OH 0.5小时并以Ar吹扫后的红外谱图)。反应条件:常压,483 K。原位红外实验结果表明,CO、甲氧基、水或其衍生物(-OH)为可能的表面主要吸附态物种,且CO主要吸附在Pt上,甲氧基和水及其衍生物种主要吸附在载体上;水的衍生物种与甲氧基等物种存在竞争吸附。▲图2 (a)以红外光谱信号为检测器,记录得到的Pt/NiAl2O4上的SSITKA(13CO+ H2O切换为12CO+ H2O)结果;(b)图(a)中t时刻CO在催化剂表面吸附的红外谱图;(c)表面物种红外特征吸收峰的归一化强度随时间的变化;(d)对(c)中脱附支曲线拟合得到的残余覆盖度方程及对应的模型。SSITKA结果表明,甲氧基吸附在两种不同的活性位点上,并且在这两种位点上的覆盖度和吸附强度不同,结合之前原位红外实验得出的结论,我们认为甲氧基主要吸附在载体上,少部分吸附在其他位点(例如Pt和NiAl2O4的界面位点);CO也以不同的覆盖度和吸附强度吸附在两种不同的位点上(主要吸附在Pt上),而水及其衍生物种吸附在单一活性位点(NiAl2O4)。▲图3 (a)总压3 MPa时,不同温度下氢气生成速率随水分压的变化;(b)483 K时产物选择性随水分压的变化曲线。氢气生成速率与水分压的相关性表明,在水分压较低时,反应主要以生成CO的甲醇脱氢过程为主,当水增加到一定量时,生成CO2的WGS过程对整体反应的影响逐渐增强。由于反应中的主要吸附态物种不变,同一温度下水对于氢气生成的反应级数变化表明反应的决速步可能发生了变化。▲图4 总压3 MPa时,不同温度条件下氢气生成速率随甲醇、CO分压的变化曲线。图4中甲醇接近于0级的反应级数以及CO负的反应级数表明,甲醇(及其衍生物)和CO在催化剂表面覆盖度相对较高,与从红外谱图中推测得到的最主要吸附态物种相一致。▲图5 Pt/NiAl2O4催化甲醇分解、WGS以及甲醇重整的动力学同位素效应汇总。▲示意图1 在Pt/NiAl2O4催化剂上进行甲醇重整的反应路径示意图。综上,甲醇重整经历甲醇脱氢以及随后的水气变换反应(WGS)过程,并经历两个分离的动力学相关步骤,分别为吸附在界面位置的甲氧基的C–H键断裂和OlH基团内的O–H键断裂(Ol:氧填充表面空位)。该反应过程的深入研究将有利于科研工作者进一步开发优质的甲醇重整催化剂,为节能减排以及“双碳”目标的实现贡献力量。